In questo articolo viene illustrata una revisione completa della finasteride, un inibitore azasteroideo dell’enzima 5 alfa-reduttasi, che alla dose di 1 mg è in commercio in Italia per il trattamento dell’alopecia androgenetica maschile. Sono dettagliate le caratteristiche farmacocinetiche e farmacodinamiche del farmaco in relazione all’alopecia androgenetica.
Conoscere la patogenesi di questa malattia è fondamentale per capire come agisce in modo specifico la finasteride, e in che modo si valutano e quando si ottengono i risultati clinici, mantenuti solo se il farmaco non è mai interrotto. Sono descritti in dettaglio gli effetti collaterali del farmaco, con una revisione critica della letteratura. Vengono infine suggerite le linee guida per impostare in modo corretto il trattamento e saper gestire il paziente al meglio nel corso di una lunga terapia.
L’alopecia androgenetica maschile
La finasteride è uno dei trattamenti di prima scelta per l’alopecia androgenetica maschile. E’ noto da anni che l’alopecia androgenetica maschile si può arrestare e migliorare solo con trattamenti medici continuati nel tempo e mai interrotti. Il trattamento deve inoltre essere iniziato negli stadi iniziali della malattia, perché le forme gravi rispondono meno alle cure, e non deve poi essere mai sospeso.
La miniaturizzazione follicolare che caratterizza la patogenesi dell’alopecia androgenetica maschile deve essere bloccata all’inizio, quando cioè il follicolo non è ancora di dimensioni troppo ridotte: solo in questo caso il trattamento medico può indurre un graduale aumento delle dimensioni del follicolo e dello spessore del capello.
Su questi presupposti si è basata per anni la ricerca scientifica di farmaci per l’alopecia androgenetica: la molecola ideale deve garantire efficacia e tollerabilità per un uso a lungo termine, e deve poter essere assunta in età giovane-adulta, all’esordio dell’alopecia androgenetica.
La finasteride, alla dose di 1 mg, è il farmaco che risponde a queste esigenze e da più di 15 anni è in commercio per il trattamento dell’alopecia androgenetica maschile in numerosi paesi del mondo: USA, Canada, Europa, Sud America e Asia. In Italia, la finasteride è disponibile in farmacia su prescrizione medica dal Marzo 1999.
La finasteride è inoltre è un trattamento “specifico” per l’alopecia androgenetica, in quanto è diretta a bloccare il meccanismo patogenetico alla base della malattia, e cioè l’effetto degli ormoni androgeni sui follicoli piliferi delle aree androgeno-dipendenti del capo.
Patogenesi dell’alopecia androgenetica: ruolo della 5-alfa reduttasi
L’alopecia è definita “andro-genetica”, in quanto per la sua comparsa sono necessari sia ormoni androgeni, che la predisposizione genetica.
Gli ormoni androgeni sono la causa principale dell’alopecia androgenetica, che per questo non compare nei soggetti castrati prima della pubertà ed è molto più frequente e grave nel sesso maschile rispetto a quello femminile. La predisposizione genetica influenza la sensibilità del follicolo agli androgeni e quindi la rapidità di sviluppo e la progressione dell’alopecia.
L’ormone androgeno responsabile dell’alopecia androgenetica è il diidrotestosterone (DHT), attivamente prodotto a livello follicolare. Il follicolo pilifero e la ghiandola sebacea sono infatti in grado di metabolizzare attivamente gli androgeni attraverso alcuni sistemi enzimatici che permettono di convertire gli androgeni deboli in derivati più potenti (5 alfa-reduttasi, 3b-idrossisteroidodeidrogenasi, 17b-idrossisteroidodeidrogenasi) e di convertire alcuni androgeni in estrogeni (aromatasi).
La 5 alfa-reduttasi è un sistema enzimatico NADPH-dipendente che catalizza la 5 alfa-riduzione del testosterone in DHT.
Nell’uomo sono presenti 3 diversi isoenzimi, la 5 alfa-reduttasi di tipo I, la 5 alfa-reduttasi di tipo II, e la 5 alfa-reduttasi di tipo III, che differiscono per distribuzione tissutale, peso molecolare e pH di attività. Poco si sa, ancora, sulle caratteristiche biochimiche della 5 alfa-reduttasi di tipo III, identificata di recente e codificata da un gene presente sul cromosoma 4q12, mentre da anni si conoscono la composizione e l’attività degli atri due isoenzimi. La 5 alfa-reduttasi di tipo I, composta da 259 aminoacidi, ha un peso molecolare di 29.5 kilodalton, è localizzata a livello microsomiale, ha un pH ottimale di 6-8.5 (anche se nelle cellule normali funziona ad un pH più neutro, di 6.0-7.0) e, nella cute, è presente soprattutto a livello delle ghiandole sebacee e sudoripare. E’ responsabile di circa 1/3 del DHT circolante. La 5 alfa-reduttasi di tipo II è composta da 254 aminoacidi, ha un peso molecolare di 28.4 kilodalton, è localizzata sia a livello microsomiale che nucleare, ha un pH ottimale di 5.5 e, nella cute, è localizzata nei follicoli piliferi, soprattutto a livello delle guaine epiteliali. All’attività della 5 alfa-reduttasi di tipo II si devono i rimanenti 2/3 del DHT circolante. I due isoenzimi sono codificati da 2 diversi geni, localizzati rispettivamente nei cromosomi 5p15 e 2p23.
Gli effetti della 5 alfa-reduttasi di tipo II e del DHT sul follicolo sono stati ben definiti dallo studio di alcune famiglie dominicane che presentavano un deficit ereditario selettivo della 5 alfa-reduttasi di tipo II. I maschi di queste famiglie, alla nascita presentavano un fenotipo femminile con genitali esterni ambigui, ma con la pubertà acquisivano un fenotipo maschile, con normale attività sessuale e fertilità, senza però sviluppare né la barba, né l’alopecia androgenetica. Questo studio ha dimostrato 3 elementi di estrema importanza:
- è il testosterone e non il DHT che regola il fenotipo maschile e la funzione sessuale dopo la pubertà;
- gli effetti del DHT dopo la pubertà si esplicano solo sui follicoli piliferi del cuoio capelluto e sulla prostata;
- la 5 alfa-reduttasi di tipo II è l’enzima cardine per lo sviluppo di alopecia androgenetica.
Studi successivi hanno confermato questi dati, mostrando che l’attività della 5 alfa-reduttasi di tipo II è molto più elevata nel maschio che non nella femmina, e in entrambi i sessi nella regione frontale (colpita dall’alopecia androgenetica) rispetto alla regione occipitale.
Il DHT, prodotto a livello follicolare dalla 5 alfa-reduttasi di tipo II, si lega al recettore specifico per gli androgeni dei follicoli, ed esercita cosi il suo effetto di indurre la miniaturizzazione follicolare e l’accorciamento della fase di crescita. E’importante ricordare che l’affinità del recettore degli androgeni per il DHT è 5-6 volte più alta di quella per il testosterone e oltre 10 volte più alta di quella per gli altri ormoni androgeni.
Per effetto del DHT, i follicoli delle aree androgeno-dipendenti iniziano il processo di miniaturizzazione, che progredisce nel tempo, con una velocità determinata dalla predisposizione genetica, e non si arresta se non trattata con farmaci specifici. Da forme iniziali di alopecia androgenetica, dove il diradamento è poco evidente, si progredisce così a forme sempre più severe, che culminano con la miniaturizzazione totale di tutti i capelli, eccezion fatta per le aree peri-auricolari e la regione nucale.
Finasteride
La finasteride è un inibitore steroideo della 5 alfa-reduttasi di tipo II: è un 4-azasteroide sintetico, con formula C23H36N2O2, creato in laboratorio per inibire la conversione del testosterone in DHT, e quindi diminuire l’attività tissutale del DHT e i suoi effetti biologici. La finasteride è assorbita molto rapidamente dopo somministrazione orale, la biodisponibilità orale è dell’80%, e non è influenzata significativamente dall’assunzione di cibo, che rallenta solo il tempo di raggiungimento della concentrazione plasmatica massima. Circa il 90% della finasteride circolante è legata a proteine plasmatiche.
Il farmaco supera la barriera emato-encefalica e si ritrova in quantità piccolissima (alcuni nanogrammi) nel liquido seminale, a livelli che non hanno significato clinico. Numerosi studi hanno mostrato l’assenza di interazioni farmacologiche con altri farmaci, per cui finasteride è prescrivibile senza particolari indicazioni di cautela se si assumono terapie concomitanti.
La finasteride si lega in modo indissolubile all’enzima 5 alfa-reduttasi di tipo II, bloccandone l’attività e 1 mg di farmaco al giorno riduce i livelli sierici di DHT del 68%, senza avere effetti significativi sul testosterone sierico. La riduzione del DHT sierico indotta dal trattamento con finasteride 1 mg non influenza la spermatogenesi. La riduzione dei livelli di DHT è già evidente dopo 2 settimane dalla somministrazione e ritorna ai valori iniziali dopo 2 settimane dalla sospensione della finasteride. Nei maschi con alopecia androgenetica, la finasteride, riduce del 65% i livelli di DHT del cuoio capelluto, le sede in cui si vuole ottenere una riduzione degli effetti di questo ormone.
L’efficacia della finasteride 1 mg nel trattamento dell’alopecia androgenetica maschile è stata dimostrata da numerosi studi clinici che hanno dimostrato che l’assunzione di 1 mg al giorno di finasteride per via orale provoca, dopo 5 anni, un miglioramento clinico nel 48% dei pazienti trattati. Un arresto della progressione dell’AGA è stato osservato nel 99% dei casi. I miglioramenti ottenuti si mantengono nel tempo solo se l’assunzione del farmaco non viene interrotta. La finasteride è efficace anche nell’alopecia androgenetica della regione frontale e nei maschi di qualsiasi età, anche se la maggior parte degli studi clinici sono stati effettuati nella fascia di età fra i 18 ed i 45 anni. Uno studio condotto su maschi di età compresa fra i 41 e i 60 anni, affetti da alopecia androgenetica, ha mostrato la superiorità della finasteride rispetto al placebo nell’indurre miglioramento clinico dell’alopecia androgenetica dopo 1 anno di cura, monitorando i risultati con le fotografie globali e con la valutazione effettuata sia dal paziente che dall’investigatore. Un altro studio che ha incluso pazienti di età dai 18 ai 60 anni ha confermato l’efficacia del farmaco anche dopo i 40 anni, ma solamente nell’area del vertice e in quella anteriore. Nei pazienti di età superiore ai 40 anni, le regioni dell’attaccatura frontale e temporale rispondono infatti poco alla terapia.
Infine, numerosi studi mostrano che il trattamento con finasteride migliora la qualità della vita dei pazienti, e uno studio recente ha riportato che il beneficio emotivo è riportato dai pazienti già dopo 6 mesi di terapia.
Fattori predittivi di risposta dell’alopecia androgenetica maschile al trattamento con finasteride 1 mg
Non si può predire quali pazienti con alopecia androgenetica maschile otterranno beneficio clinico dal trattamento con finasteride 1 mg, quali assisteranno ad un arresto della progressione della malattia, e quali non risponderanno alla cura. Le forme lievi di alopecia androgenetica rispondono meglio alla terapia. Anche se i miglioramenti clinici sono a volte già evidenti dopo alcuni mesi di cura, la valutazione dell’efficacia deve essere fatta dopo 1 anno di trattamento ininterrotto, ed il giudizio di efficacia è più obiettivo se oltre alle foto globali si paragonano le foto con videodermatoscopio a ingrandimenti di 10-20x.
E’ sempre necessario spiegare sin dall’inizio al paziente che la terapia con finasteride 1 mg non deve mai essere sospesa, e che a tutt’oggi non esistono cure per l’alopecia androgenetica che permettano di mantenere nel tempo gli effetti benefici se interrotte.
Terapie di associazione
I due farmaci in commercio in Italia per il trattamento dell’alopecia androgenetica maschile sono la finasteride 1 mg in compresse e il minoxidil al 5% in lozione, che hanno meccanismi di azione diversi e possono pertanto essere utilizzati in associazione per aumentare l’efficacia della terapia. L’esperienza clinica, supportata da alcuni studi, ha mostrato effetti benefici dal trattamento combinato finasteride 1 g con minoxidil 5% lozione, che è suggerito quando dopo 1 anno di cura con uno dei due farmaci il paziente non è soddisfatto dall’efficacia, o nelle forme gravi di alopecia androgenetica (grado IV della scala di Hamilton-Norwood) che hanno poche possibilità di risposta.
La finasteride è spesso prescritta ai pazienti con alopecia androgenetica in attesa di autotrapianto di capelli, in quando gli effetti benefici del farmaco sui follicoli inducono una riduzione dell’area colpita dall’alopecia androgenetica, con necessità di trapianto di un minor numero di unità follicolari. La finasteride inoltre protegge i follicoli originali dal processo di miniaturizzazione, garantendo una migliore riuscita nel tempo del trattamento chirurgico.
Effetti collaterali
Raramente (<2% dei pazienti), la finasteride 1 mg può provocare disturbi a carico della sfera sessuale (diminuzione della libido, del volume dell’eiaculato, difficoltà dell’erezione). Gli studi clinici controllati dimostrano che tutti questi effetti sono tuttavia totalmente reversibili alla sospensione della terapia e talvolta scompaiono anche continuando il trattamento. Le ragioni per la comparsa degli effetti collaterali sessuali, che si manifestano entro i primi 2-3 mesi di cura, possono essere l’aumento degli estrogeni, per effetto della trasformazione del testosterone in estradiolo da parte dell’aromatasi o la diminuzione del DHT a livello cerebrale.
La sicurezza e l’efficacia della finasteride sono state recentemente confermate da una meta-analisi di studi clinici controllati sull’alopecia androgenetica maschile.
La finasteride nella donna
La finasteride è utilizzata da anni nelle donne in età fertile per il trattamento dell’irsutismo, associato o non a sindrome dell’ovaio policistico. La terapia, sempre effettuata assieme al contraccettivo orale, è considerata di seconda scelta e necessita di 5 mg al giorno di finasteride. Nel trattamento dell’alopecia androgenetica femminile, la finasteride è stata provata con successo nelle donne in pre e post-menopausa, senza iperandrogenismo, alla dose di 5 mg al giorno. Il trattamento con finasteride 5 mg ha aumentato la densità e il diametro dei capelli, valutati con il fototricogramma e la fotografia globale dopo almeno 1 anno di trattamento.
Bibliografia
- Gan DC, Sinclair RD. Prevalence of male and female pattern hair loss in Maryborough. J Investig Dermatol Symp Proc. 2005;10:184–9.
- Guarrera M, Rebora A. Kenogen in female androgenetic alopecia. A longitudinal
study. Dermatology. 2005;210(1):18-20. - Heilmann S, Brockschmidt FF, Hillmer AM, Hanneken S, Eigelshoven S, Ludwig KU, Herold C, Mangold E, Becker T, Kruse R, Knapp M, Nöthen MM. Evidence for a polygenic contribution to androgenetic alopecia. Br J Dermatol. 2013;169(4):927-30.
- Thigpen AE, Silver RI, Guileyardo JM, Casey ML, McConnell JD, Russell DW. Tissue distribution and ontogeny of steroid 5 alpha-reductase isozyme expression. J Clin Invest. 1993;92:903–910.
- Azzouni F, Godoy A, Li Y, Mohler J. The 5 alpha-reductase isozyme family: a review of basic biology and their role in human diseases. Adv Urol. 2012;2012:530121.
- Imperato-McGinley J, Guerrero L, Gautier T, Peterson RE. Steroid 5alpha-reductase deficiency in man: an inherited form of male pseudohermaphroditism. Science. 1974;186:1213-5.
- Sawaya ME, Price VH. Different levels of 5alpha-reductase type I and II, aromatase, and androgen receptor in hair follicles of women and men with androgenetic alopecia. J Invest Dermatol 1997;109: 296-300.
- Budd D, Himmelberger D, Rhodes T et al. The effects of hair loss in European men: a survey in four countries. European Journal of Dermatology 2000;10:122-7.
- Han SH, Byun JW, Lee WS, et al. Quality of life assessment in male patients with androgenetic alopecia: result of a prospective, multicenter study. Ann Dermatol. 2012;24:311–8.
- Lasseter K: An open-label, multiple-dose study to investigate the pharmakokinetics of finasteride 1 mg administered orally in healthy adult male subjects. MRL clinical study report; Merck Research laboratories 1997; protocol 102 (data on file).
- Carlin JR; Hoglund P, Eriksson L-O, et al: Disposition and pharmakokynetics of [14C]finasteride after oral administration in humans. Drug Metab Dispos 1992;20:148-155.
- Propecia (finasteride) original NDA application clinical documentation. Merck Research Laboratories. D. clinical efficacy and safety, Volume 1, 23 (data on file).
- Kaufman KD, Olsen EA, Whiting D, et al. Finasteride in the treatment of men with androgenetic alopecia. Finasteride Male Pattern Hair Loss Study Group. J Am Acad Dermatol. 1998;39:578-89.
- Dallob AL, Sadick NS, Unger W, et al. The effect of finasteride, a 5 alpha-reductase inhibitor, on scalp skin testosterone and dihydrotestosterone concentrations in patients with male pattern baldness. J Clin Endocrinol Metab. 1994;79:703-6.
- Drake L, Hordinsky M, Fiedler V, et al. The effects of finasteride on scalp skin and serum androgen levels in men with androgenetic alopecia. J Am Acad Dermatol. 1999;41:550-4.
- McClellan KJ, Markham A. Finasteride: a review of its use in male pattern hair loss. Drugs. 1999;57:111-26.
- Rittmaster RS, Antonian L, New MI, Stoner E. Effect of finasteride on adrenal
steroidogenesis in men. J Androl. 1994;15:298-301. - Rittmaster RS, Lemay A, Zwicker H, et al. Effect of finasteride, a 5 alpha-reductase inhibitor, on serum gonadotropins in normal men. J Clin Endocrinol Metab. 1992;75:484-8.
- MRL clinical study report, multicenter study: a double-blind, randomized, placebo-controlled multicenter study to evaluate the safety of low-dose finasteride in male volunteers. Merck Research Laboratories 1996 (protocol 094) (data on file).
- Andriole GL, Guess HA, Epstein JI, et al, PLESS Study Group. Treatment with finasteride preserves usefulness of prostate-specific antigen in the detection of prostate cancer: results of a randomized, double-blind, placebocontrolled clinical trial. Urology. 1998;52:195-201.
- Canfield D. Photographic documentation of hair growth in androgenetic alopecia. Dermatol Clin 1996;14:713-21.The Finasteride Male Pattern Hair Loss Study Group. Long-term (5-year) multinational experience with finasteride 1 mg in the treatment of men with androgenetic alopecia. Eur J Dermatol 2002;12:38-49.
- Kaufman KD, Girman CJ, Round EM, et al. Progression of hair loss in men with androgenetic alopecia (male pattern hair loss): long-term (5-year) controlled observational data in placebo-treated patients. Eur J Dermatol 2008;18:407-11.
- Kaufman KD, Rotonda J, Shah AK, Meehan AG. Long-term treatment with finasteride 1 mg decreases the likelihood of developing further visible hair loss in men with androgenetic alopecia (male pattern hair loss). Eur J Dermatol 2008;18:400-6.
- Leyden J, Dunlap F, Miller B, Winters P, Lebwohl M, Hecker D, et al. Finasteride in the treatment of men with frontal male pattern hair loss. J Am Acad Dermatol 1999;40:930-7.
- Whiting DA, Olsen EA, Savin R, et al. Efficacy and tolerability of finasteride 1 mg in men aged 41 to 60 years with male pattern hair loss. Eur J Dermatol 2003;13:150-60.
- Olsen EA, Whiting DA, Savin R, et al. Global photographic assessment of men aged 18 to 60 years with male pattern hair loss receiving finasteride 1mg or placebo. J Am Acad Dermatol 2012;67:379-386.
- Kawashima M, Hayashi N, Igarashi A, et al. Finasteride in the treatment of Japanese men with male pattern hair loss. Eur J Dermatol 2004; 14:247-254.
- Price VH, Menefee E, Sanchez M, Kaufman KD. Changes in hair weight in men with androgenetic alopecia after treatment with finasteride (1mg daily): three and 4-year results. J Am Acad Dermatol 2006;55:71-74.
- Whiting DA, Waldstreicher J, Sanchez M, Kaufman KD. Measuring reversal of hair miniaturization in androgenetic alopecia by follicular counts in horizontal sections of serial scalp biopsies: results of finasteride 1 mg treatment of men and postmenopausal women. J Investig Dermatol Symp Proc. 1999;4:282-284.
- Kaufman KD. Androgens and alopecia. Mol Cell Endocrinol. 2002;198:89-95.
- Yamazaki M, Miyakura T, Uchiyama M, et al. Oral finasteride improved the quality of life of androgenetic alopecia patients. J Dermatol 2011;38:773-777.
- Inadomi T. Efficacy of finasteride for treating patients with androgenetic alopecia who are pileous in other areas: a pilot study in Japan. Indian J Dermatol 2014; 59:163-165.
- Rossi A, Cantisani C, Scarno M, et al. Finasteride 1mg daily administration on male androgenetic alopecia in different age groups: 10-year follow-up. Dermatol Ther 2011; 24:455-461.
- Mella JM, Perret MC, Manzotti M, et al. Efficacy and safety of finasteride therapy for androgenetic alopecia: a systematic review. Arch Dermatol 2010;146:1141-1150.
- Irwig MS. Persistent sexual side effects of finasteride: could they be permanent? J Sex Med 2012; 9:2927-2932.
- Irwig MS, Kolukula S. Persistent sexual side effects of finasteride for male pattern hair loss. J Sex Med 2011; 8:1747-1753.
- Gupta AK, Charrette A. The efficacy and safety of 5alpha-reductase inhibitors in androgenetic alopecia: a network meta-analysis and benefit-risk assessment of finasteride and dutasteride. J Dermatol Treat 2014;25:156–161.
- Mansouri P, Farshi S, Safar F. Finasteride-induced gynecomastia. Indian J Dermatol Venereol Leprol 2009; 75:309–310.
- Ramot Y, Czarnowicki T, Zlotogorski A. Finasteride induced gynecomastia: case report and review of the literature. Int J Trichol 2009; 1:27-29.
- Bird ST, Brophy JM, Hartzema AG, et al. Male breast cancer and 5alphareductase inhibitors finasteride and dutasteride. J Urol 2013; 190:1811-1814.
- Traish AM, Hassani J, Guay AT, et al. Adverse side effects of 5alphareductase inhibitors therapy: persistent diminished libido and erectile dysfunction and depression in a subset of patients. J Sex Med 2011; 8:872-884.
- Irwig MS. Depressive symptoms and suicidal thoughts among former users of finasteride with persistent sexual side effects. J Clin Psychiatry 2012; 73:1220-1223.
- Altomare G, Capella GL. Depression circumstantially related to the administration of finasteride for androgenetic alopecia. J Dermatol 2002; 29:665-669.
- Finn DA, Beadles-Bohling AS, Beckley EH, et al. A New Look at the 5alfa-Reductase Inhibitor Finasteride. Drug Reviews 2006; 12: 53-76.
- Somani N, Turvy D. Hirsutism: an evidence-based treatment update. Am J Clin Dermatol. 2014;15:247-66.
- Tartagni MV, Alrasheed H, Damiani GR, et al. Intermittent low-dose finasteride administration is effective for treatment of hirsutism in adolescent girls: a pilot study. JPediatr Adolesc Gynecol. 2014;27:161-5.
- Yeon JH, Jung JY, Choi JW, et al. 5 mg/day finasteride treatment for normoandrogenic Asian women with female pattern hair loss. J Eur Acad Dermatol Venereol 2011; 25:211-214.
- Oliveira-Soares R, E Silva JM, Correia MP, André MC. Finasteride 5 mg/day Treatment of Patterned Hair Loss in Normo-androgenetic Postmenopausal Women. Int J Trichology. 2013;5:22-5.
- Yim E, Nole KL, Tosti A. 5 alpha-reductase inhibitors in androgenetic alopecia. Curr Opin Endocrinol Diabetes Obes 2014; 21:493-498.
- Piraccini BM, Alessandrini A. Androgenetic alopecia. G Ital Dermatol 2014; 149:15-24.

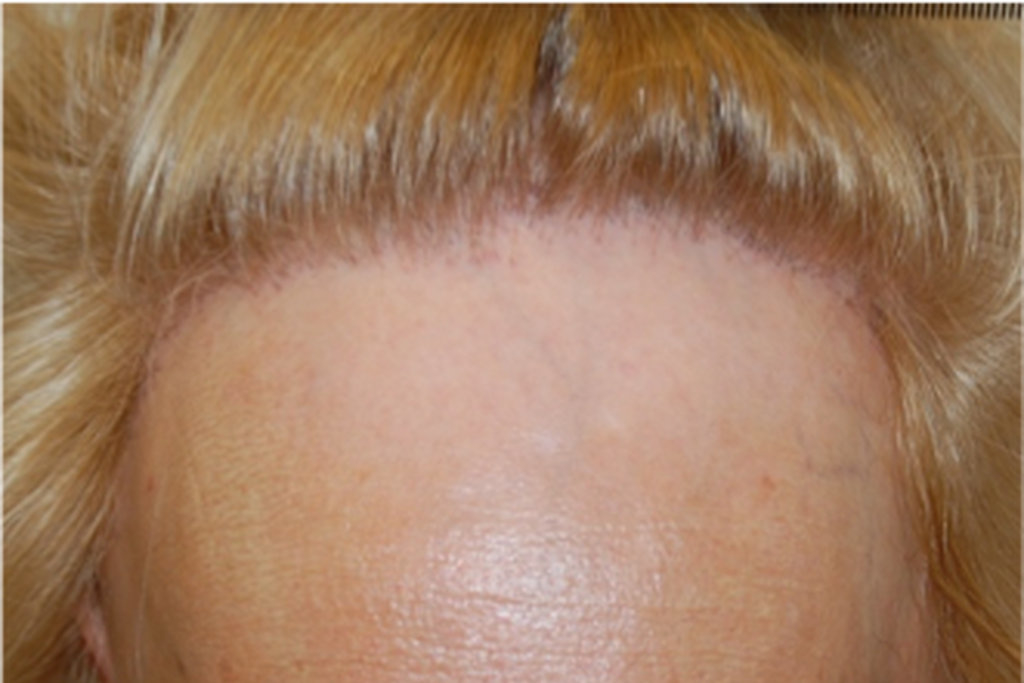
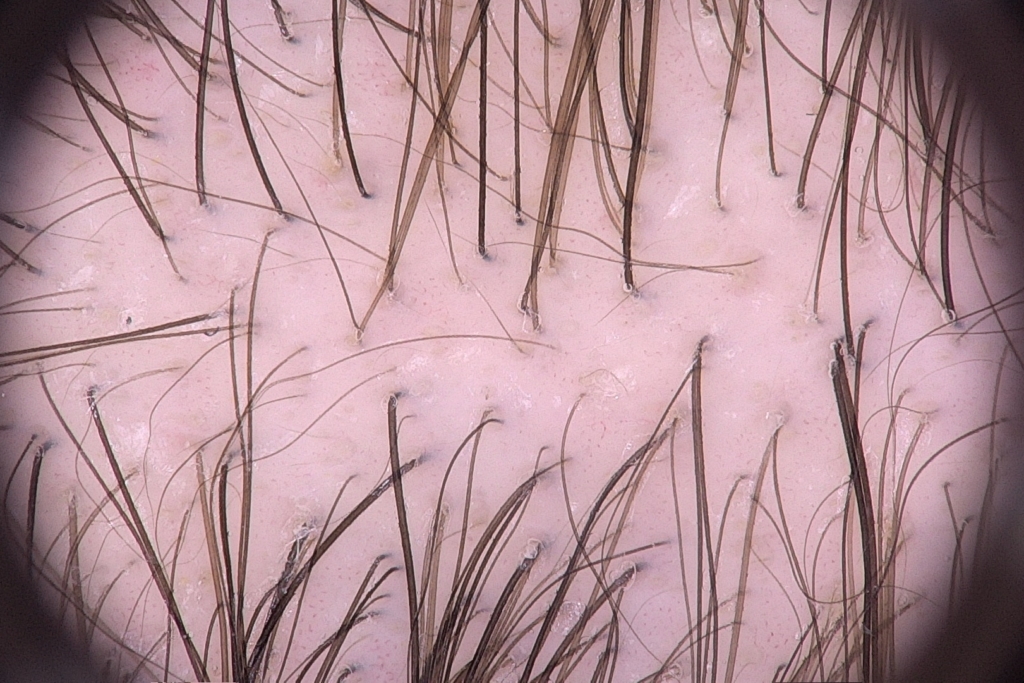

Gentile Dott.ssa Piraccini, scrivo per chiedere un Suo autorevole parere.
Sono un uomo di 35 anni affetto da alopecia androgenetica. Circa 5 anni fa ho iniziato ad assumere finasteride 1 mg/die per poi passare dopo 1 anno a spezzare la compressa da 5 mg in 4-5 parti (anche a seguito del consiglio del mio medico di base), al fine di evitare il grosso esborso economico del farmaco originale. Dopo 2 anni e mezzo di assunzione della finasteride, ho dovuto interrompere la cura perché si sono verificati diversi effetti collaterali: diminuzione della libido, del volume dell’eiaculato in maniera massiccia, e infine difficoltà dell’erezione.
Inutile dire che la capigliatura è peggiorata davvero. Nonostante infatti l’utilizzo costante di minoxidil, da 3 anni a questa a parte i capelli sono finissimi, oltre ad averne persi molti nell’area fronto parietale.
Chiedo se a suo avviso, può essere utile ritentare la terapia con finasteride 1 mg/die, oppure debbo mettermi l’anima in pace perché evidentemente faccio parte di quei pazienti che non sono buoni candidati al farmaco. Sono molto sconfortato onestamente.
La ringrazio molto per ogni riscontro voglia darmi e le auguro buon lavoro.
Buongiorno,
non è facile rispondere alla sua domanda perché per darle un parare sono necessarie più informazioni ed una visita per vedere la situazione dei suoi capelli.
I miei dubbi riguardano il fatto che la finasteride abbia indotto gli effetti collaterali dopo tanti anni di trattamento, cosa inusuale, e che il minoxidil non sia efficace, quindi mi chiedo cosa e come lo utilizza. Se vuole venire a una visita ne parliamo.
Cordialità
Bmpiraccini
Buon giorno Dottoressa, sono un uomo di 45, volevo chiederle se posso fare uso della Propecia,anche alla mia età?
gentile Roberto, la finasteride e’ efficace a tutte le età, ma dopo i 40 ci si aspetta meno risultati. E’ comunque necessaria una valutazione individuale per capire cosa e’ meglio fare come terapia in ogni singolo paziente
Cordialità bmpiraccini
Gentile dottoressa Piraccini, tempo fa le scrissi in merito ad un mio dubbio sull’efficacia del minoxidil rispetto alla finasteride sulla regione frontale, e lei fu così gentile da rispondermi; pertanto approfitto per sottoporle un altro quesito. Come forse lei stessa saprà, ultimamente si fa un gran parlare di un nuovo integratore a base di procianidine B2 dell’estratto secco di mela annurca sintetizzato da un gruppo di ricerca dell’Università Federico II di Napoli. In effetti, già all’inizio degli anni 2000, un gruppo di ricerca giapponese stabilì l’efficacia di questi polifenoli nel trattamento dell’alopecia androgenetica mediante applicazione topica, dato che sembra che queste molecole siano in grado di bloccare i fattori apoptotici stimolati dal DHT, quindi agirebbero a valle del processo di miniaturizzazione dei capelli, a differenza della finasteride, che invece agirebbe a monte, inibendo direttamente la conversione del testosterone in DHT. Mi piacerebbe conoscere la sua opinione in merito. Per completezza, le allego il link allo studio prodotto dal gruppo napoletano:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5775114/pdf/jmf.2017.0016.pdf
Cordiali saluti.
Giuseppe
Gentile Dottoressa,
Ho letto con interesse l’articolo che ho trovato solo ora e, pur seguendo da anni informazioni relative alla Finasteride, ho ancora qualche dubbio sul processo di crescita dei capelli.
Prendendo Finasteride per anni fino a circa 30 anni di eta’ sono riuscito a mantenere ottimi capelli. Dopodiche’ ho smesso per circa 5 anni e negli ultimi 2 ho notato un peggiornamento, quindi ho ripreso.
Sto cercando di capire quanto quei 5 anni senza Finasteride abbiano influito sulla capacita’ dei capelli di riprendersi e migliorare avendo iniziato di nuovo la cura, poiche’ la perdita di capelli e’ stata veramente lenta dopo i 30 anni e senza Finasteride.
Ora, a 2 anni di inizio, ho notato miglioramenti, ma vorrei capire se in quei 5 anni precedenti alcuni capelli possano essere arrivati ad uno stadio di vellus e non riescano a riprendere spessore e colore.
Due domande:
E’ verosimile che con una caduta cosi’ lenta senza Finasteride, la maggior parte dei capelli tornera’ come prima e ricrescera’? Alcuni dermatologi mi hanno detto che e’ plausibile, ma ho anche letto che ci sono fasi della vita in cui comunque si hanno brusche perdite di capelli, tipo a circa 25 anni, poi a 35 e a 38 e con o senza farmaci e’ impensabile avere i capelli di un diciottenne.
Come fare a contrastare gli effetti collaterali di Minoxidil associato alla cura quali brufoli e un senso di oppressione al torace?
Non vedo risposte da nessuna parte in rete o da dermatologi perche’ mi viene sempre detto che ogni alopecia segue il suo corso.
La ringrazio per il suo commento se vorra’ chiarire questi punti come estensione dell’articolo pubblicato sopra.
Buonasera.
Gentile Matteo,
La ringrazio del commento e delle domande. Dopo 2 anni di ripresa della cura con finasteride ha oramai ottenuto il miglioramento massimo ottenibile con il farmaco, e quello che ha perso nei 5 anni di interruzione della cura non può essere più ripreso con questo trattamento.
Il minoxidil lozione non provoca brufoli, né oppressione al torace. certo è che ogni effetto che compare durante un trattamento è da valutare con una visita ed un colloquio e non con una semplice mail!
cordialità bmpiraccini
Salve dottoressa, articolo molto interessante. Sono un ragazzo di 22 anni affetto da alopecia androgenetica, i danni maggiori li ho avuti nella zona tempie e nella parte frontale dove ho visto un arretramento delle tempie e un diradamento della parte frontale, ma anche un diradamento generale il tutto successo nel giro di 4-5 mesi. Da 6 mesi e più prendo finasteride equivalente da 1mg, devo dire che la situazione generalmente è migliorata tantissimo. Nella zona tempie e nella parte frontale ( le zone più colpite) ho visto rinascere capelli più sani e forti. Nella zona dove ho recuperato cm nelle tempie peró rispetto al resto i capelli sono piu diradati. Quello che mi chiedo è se continuando con la cura ho speranze di rinfoltire anche la zona recuperata dopo lassunzione finasteride e se ho ancora margini di miglioramento. Grazie
Gentile Nunzio, il miglioramento indotto dalla finasteride aumenta nel tempo,nei primi 1-2 anni di cura.non avendola mai vista, pero, non posso rispondere in modo specifico alla sua domanda. Cordilaità bmpiraccini